宋主任解读《药品经营质量管理规范现场检查指导原则》(一)
日期:2017/6/19
6月16日应上海医药商业行业协会邀请,上海药品审评核查中心宋宝珠主任为本市药品企业进行了一场贯彻实施国家总局《药品经营质量管理规范现场检查指导原则》培训,原定250人的培训增加到400多人。历时近4个小时的培训,宋主任详细讲解了《指导原则》和现场检查的要点,并根据企业提出的问题进行了解答。为帮助企业理解、掌握《指导原则》,我们整理编辑本次培训的内容,未经本人校对,仅供企业参考。由于篇幅较长,将分期登载,敬请关注。

-
原《上海市药品经营质量管理现场检查评定细则》(2014版)停止执行。
-
《药品经营质量管理规范现场检查指导原则》5月1日全面实施,12月31日前全部整改到位。
-
《评定细则》与《指导原则》相比要求有高有低,实施《指导原则》后采取就高原则。


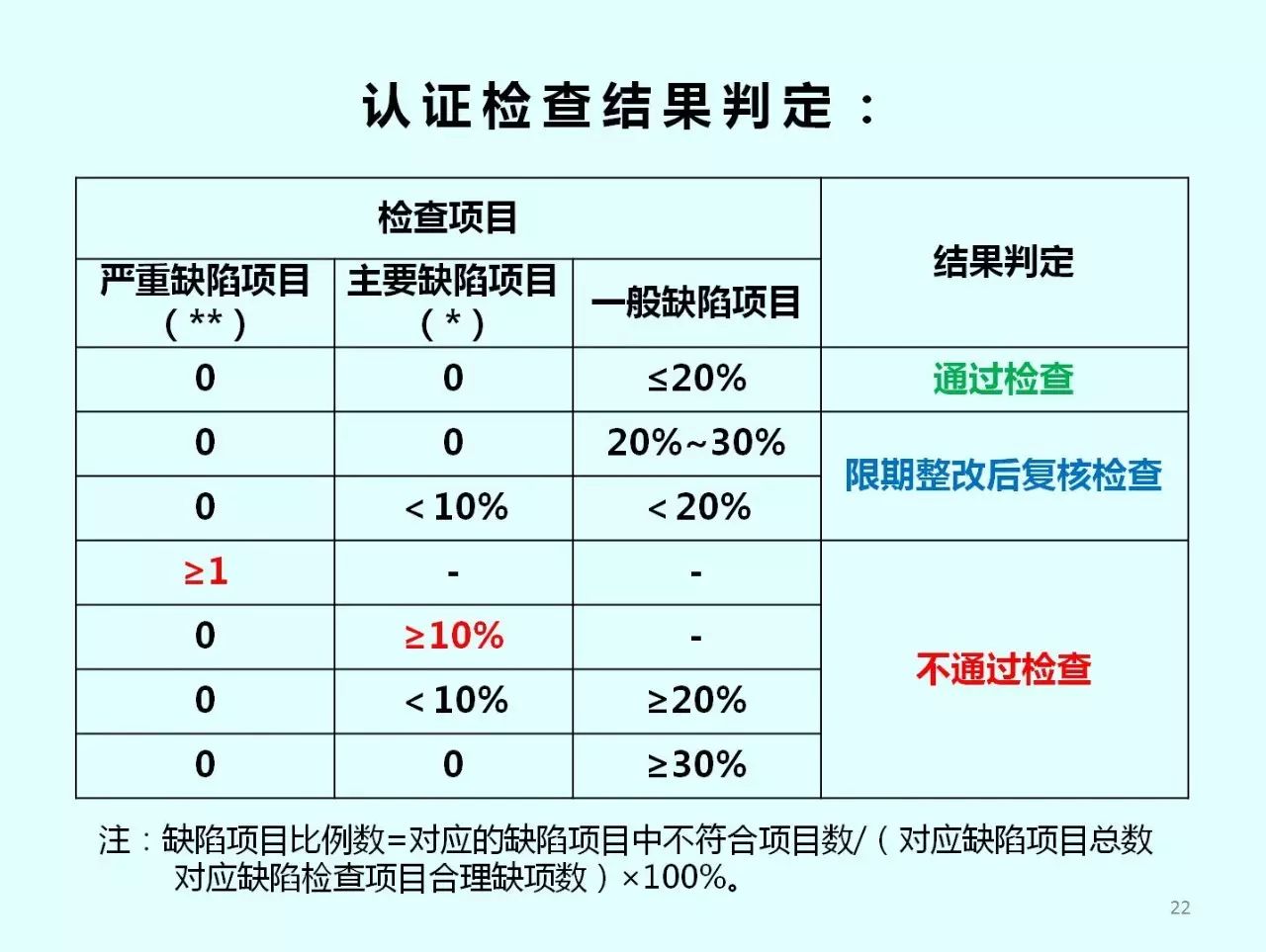
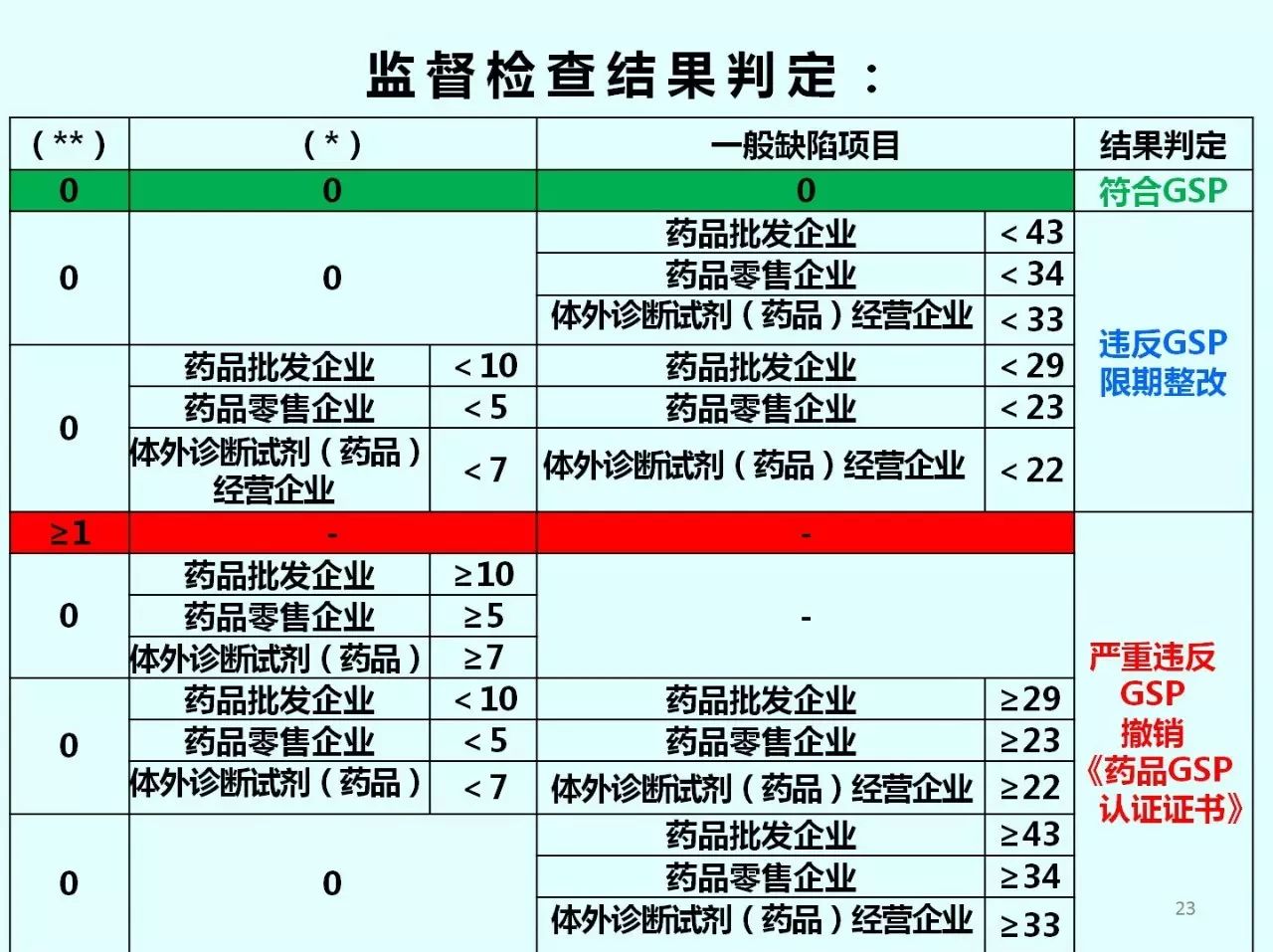
总则**00201
• 企业应当在药品采购、储存、销售、运输等环节采取有效的质量控制措施,确保药品质量,并按照国家有关要求建立药品追溯系统,实现药品可追溯。
总则**00402
• 药品经营企业应当坚持诚实守信,禁止任何虚假、欺骗行为。
〈解读〉
1、企业人员应当如实回答检查人员提问,协助完成现场检查。
2、企业提供资料应客观真实,不得隐瞒、编造。
如:企业未如实提供部分资料:备用发电机组未连线;
部分运输单上信息非运货人员本人填写;
擅自更改药品库存销售情况等。
机构与质量管理职责*00701
• 企业质量管理体系应当与其经营范围和规模相适应,包括组织机构、人员、设施设备、质量管理体系文件及相应的计算机系统等。
〈解读〉
1、药品零售连锁企业至少应设置质量管理、门店管理、人事管理等机构,具体负责企业经营质量、员工培训和健康检查等管理工作。
2、批发经营场所应包括:总经理室、人事、财务、业务、质量等各主要部门
如:质量管理体系与其经营范围经营规模不相适应
质量管理体系*00901
• 应当对内审的情况进行分析,依据分析结论制定相应的质量管理体系改进措施,不断提高质量控制水平,保证质量管理体系持续有效运行。
〈解读〉
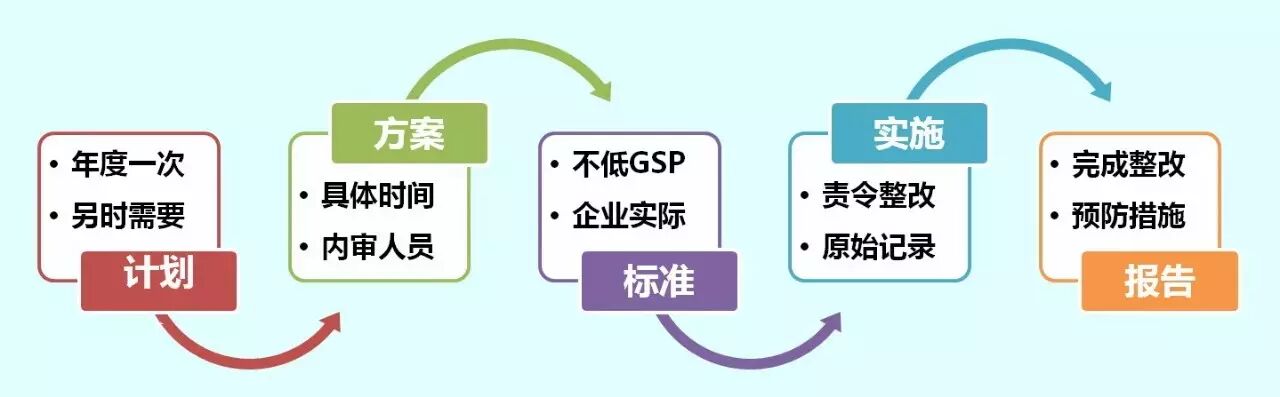
1、计算机系统进行升级,功能完善。
2、质量管理体系文件及时修改
如:未根据质量体系审核管理制度规定的要求开展年度内审:
1.“质量体系审核(GSP内部评审)报告”未经总经理批准;
2. 无法提供2017年度评审计划;
3.未对 “质量体系审核(GSP内部评审)报告”中提出的不足按制度要求采取纠正或预防措施。
人员与培训*02101
• 企业质量管理部门负责人应当具有执业药师资格和3年以上药品经营质量管理工作经历,能独立解决经营过程中的质量问题。
〈解读〉
• 企业质量管理部门负责人:
-
应有大学专科以上学历
-
执业药师资格
-
3年以上药品经营质量管理工作经历
如:质量管理部门负责人资质不符合要求
人员与培训*02301
• 从事质量管理、验收工作的人员应当在职在岗,不得兼职其他业务工作。
〈解读〉
• 质量负责人(可兼企业负责人等)、
• 质量管理部门负责人(不兼)、
• 质量员(不兼)、
• 验收员(兼收货)。
• 如:国家局飞检。
人员与培训*02501*02801*02802
• 企业应当对各岗位人员进行与其职责和工作内容相关的岗前培训和继续培训,以符合《规范》的要求。
• 从事特殊管理药品的人员,应当接受相关法律法规和专业知识培训并经考核合格后方可上岗。
• 从事冷藏冷冻药品储存、运输等工作的人员,应当接受相关法律法规和专业知识培训并经考核合格后方可上岗。
〈解读〉
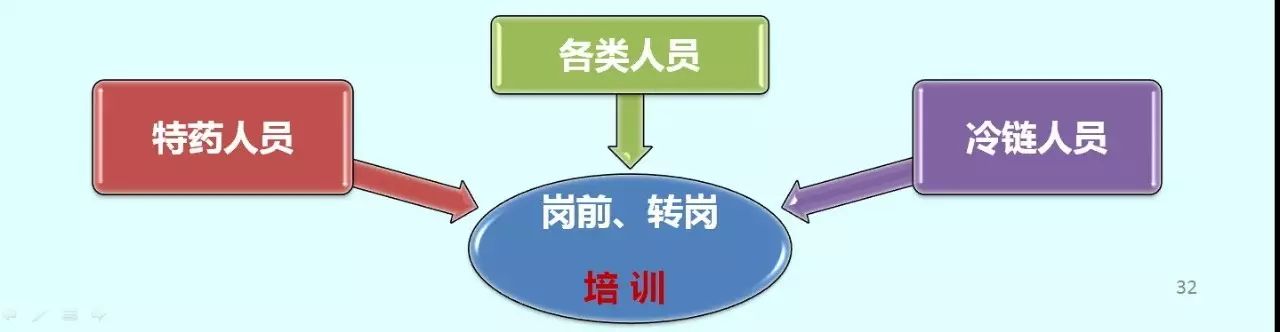
如:个别转岗人员未进行岗前培训:验收人员xxx于2017年4月16日上岗,未对其进行与职责和工作内容相关的岗前培训,现场检查时该验收人员对收货与验收操作流程及计算机操作系统不熟悉。
6月16日应上海医药商业行业协会邀请,上海药品审评核查中心宋宝珠主任为本市药品企业进行了一场贯彻实施国家总局《药品经营质量管理规范现场检查指导原则》培训,原定250人的培训增加到400多人。历时近4个小时的培训,宋主任详细讲解了《指导原则》和现场检查的要点,并根据企业提出的问题进行了解答。为帮助企业理解、掌握《指导原则》,我们整理编辑本次培训的内容,未经本人校对,仅供企业参考。由于篇幅较长,将分期登载,敬请关注。

-
原《上海市药品经营质量管理现场检查评定细则》(2014版)停止执行。
-
《药品经营质量管理规范现场检查指导原则》5月1日全面实施,12月31日前全部整改到位。
-
《评定细则》与《指导原则》相比要求有高有低,实施《指导原则》后采取就高原则。




总则**00201
• 企业应当在药品采购、储存、销售、运输等环节采取有效的质量控制措施,确保药品质量,并按照国家有关要求建立药品追溯系统,实现药品可追溯。
总则**00402
• 药品经营企业应当坚持诚实守信,禁止任何虚假、欺骗行为。
〈解读〉
1、企业人员应当如实回答检查人员提问,协助完成现场检查。
2、企业提供资料应客观真实,不得隐瞒、编造。
如:企业未如实提供部分资料:备用发电机组未连线;
部分运输单上信息非运货人员本人填写;
擅自更改药品库存销售情况等。
机构与质量管理职责*00701
• 企业质量管理体系应当与其经营范围和规模相适应,包括组织机构、人员、设施设备、质量管理体系文件及相应的计算机系统等。
〈解读〉
1、药品零售连锁企业至少应设置质量管理、门店管理、人事管理等机构,具体负责企业经营质量、员工培训和健康检查等管理工作。
2、批发经营场所应包括:总经理室、人事、财务、业务、质量等各主要部门
如:质量管理体系与其经营范围经营规模不相适应
质量管理体系*00901
• 应当对内审的情况进行分析,依据分析结论制定相应的质量管理体系改进措施,不断提高质量控制水平,保证质量管理体系持续有效运行。
〈解读〉

1、计算机系统进行升级,功能完善。
2、质量管理体系文件及时修改
如:未根据质量体系审核管理制度规定的要求开展年度内审:
1.“质量体系审核(GSP内部评审)报告”未经总经理批准;
2. 无法提供2017年度评审计划;
3.未对 “质量体系审核(GSP内部评审)报告”中提出的不足按制度要求采取纠正或预防措施。
人员与培训*02101
• 企业质量管理部门负责人应当具有执业药师资格和3年以上药品经营质量管理工作经历,能独立解决经营过程中的质量问题。
〈解读〉
• 企业质量管理部门负责人:
-
应有大学专科以上学历
-
执业药师资格
-
3年以上药品经营质量管理工作经历
如:质量管理部门负责人资质不符合要求
人员与培训*02301
• 从事质量管理、验收工作的人员应当在职在岗,不得兼职其他业务工作。
〈解读〉
• 质量负责人(可兼企业负责人等)、
• 质量管理部门负责人(不兼)、
• 质量员(不兼)、
• 验收员(兼收货)。
• 如:国家局飞检。
人员与培训*02501*02801*02802
• 企业应当对各岗位人员进行与其职责和工作内容相关的岗前培训和继续培训,以符合《规范》的要求。
• 从事特殊管理药品的人员,应当接受相关法律法规和专业知识培训并经考核合格后方可上岗。
• 从事冷藏冷冻药品储存、运输等工作的人员,应当接受相关法律法规和专业知识培训并经考核合格后方可上岗。
〈解读〉

如:个别转岗人员未进行岗前培训:验收人员xxx于2017年4月16日上岗,未对其进行与职责和工作内容相关的岗前培训,现场检查时该验收人员对收货与验收操作流程及计算机操作系统不熟悉。
信息来源:上海医药商业行业协会
|